Đại diện Học viện Quân y ngày 28/9 cho biết đã hoàn chỉnh hồ sơ bổ sung để xin cấp phép khẩn cấp vaccine Nanocovax, gửi Bộ Y tế.
Tuy nhiên, đại diện Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, cho biết chưa nhận được các hồ sơ cập nhật do nhóm nghiên cứu vaccine nộp, vì vậy chưa thể thẩm định hồ sơ của vaccine Nanocovax.
Cuộc họp gần nhất là hôm 18/9, Hội đồng Đạo đức đánh giá vaccine Covid-19 Nanocovax "đạt yêu cầu về tính an toàn, chưa có dữ liệu đánh giá hiệu lực bảo vệ".
Theo trình tự, hồ sơ hoàn chỉnh cùng biên bản nghiệm thu từ Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia sẽ được Cục Quản lý Dược chuyển Hội đồng Tư vấn xem xét.
Nếu được thông qua, Hội đồng Tư vấn sẽ đề xuất Bộ Y tế cấp phép khẩn cấp cho Nanocovax. Sau đó, vaccine chỉ được sử dụng có điều kiện theo số lượng và kế hoạch được Bộ Y tế phê duyệt. Hội đồng Tư vấn cũng có thể không thông qua, tiếp tục yêu cầu nhà sản xuất bổ sung hồ sơ.
Thông thường, một vaccine mới phải mất khoảng 5 năm từ nghiên cứu đến thử nghiệm, cấp phép. Trong những tình huống đặc biệt, như đại dịch Covid-19, vaccine có thể được cấp phép khẩn cấp nhằm kịp thời đưa vào tiêm chủng dù chưa hoàn thành toàn bộ quy trình thử nghiệm. Sau khi đã đủ hồ sơ dữ liệu, vaccine có thể tiến tới được cấp phép chính thức (hoàn toàn). Hiện trên thế giới, chỉ mới vaccine của hãng Pfizer được cấp phép hoàn toàn.
Theo Bộ Y tế, trong bối cảnh Covid-19 bùng phát rộng trên toàn thế giới, việc cấp phép khẩn cấp cho một loại vaccine là điều cần thiết dù chưa đủ thời gian để theo dõi trong thời gian dài như thông lệ. Tuy nhiên, để đảm bảo tính an toàn của vaccine, vẫn phải thực hiện đầy đủ quy trình đánh giá hiệu quả bảo vệ.
Như thông lệ quốc tế, tất cả vaccine Covid-19 trước khi đưa vào sử dụng khẩn cấp tại Việt Nam, kể cả vaccine nước ngoài và nội địa, đều phải tuân thủ thử nghiệm lâm sàng qua 3 giai đoạn, trên nguyên tắc đảm bảo 3 yếu tố: An toàn, sinh miễn dịch và quan trọng nhất là hiệu quả bảo vệ.
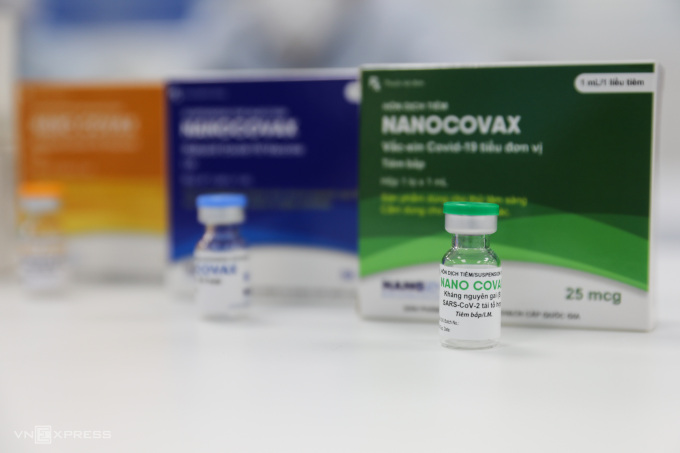 Vaccine Nanocovax tại nhà máy của Công ty Nanogen trong khu công nghệ cao TP HCM, ngày 23/6. Ảnh: Quỳnh Trần
Vaccine Nanocovax tại nhà máy của Công ty Nanogen trong khu công nghệ cao TP HCM, ngày 23/6. Ảnh: Quỳnh Trần
Nanocovax là vaccine Covid-19 do Công ty Nanogen nghiên cứu, phát triển, có một liệu trình hai liều tiêm. Giai đoạn 3 thử nghiệm lâm sàng bắt đầu từ 11/6, chia thành hai pha gồm 3a thử nghiệm trên 1.004 người tình nguyện ở Hà Nội và Long An, theo tỷ lệ cứ 6 người tiêm vaccine thì có một người tiêm giả dược; 3b thử nghiệm trên 12.000 người, tỷ lệ hai người tiêm vaccine, một người tiêm giả dược, tại Hà Nội, Hưng Yên, Long An, Tiền Giang.
Thử nghiệm được làm mù, tức nghiên cứu viên và người tình nguyện không biết ai được tiêm vaccine, ai được tiêm giả dược. Tỷ lệ các nhóm tuổi tham gia nghiên cứu lâm sàng giai đoạn 3a là 60% người từ 18-45 tuổi, 22% từ 46-60 tuổi, hơn 17% còn lại là nhóm trên 60 tuổi.
Hiện các tình nguyện viên đã được tiêm đủ hai liều, bước vào quá trình đánh giá, theo dõi. Báo cáo giữa kỳ pha 3a và 3b đã được Nanogen gửi tới Bộ Y tế, được Hội đồng Đạo đức thẩm định hai lần vào 22/8 và 18/9, đồng ý sử dụng các kết quả nghiên cứu để xem xét cấp phép khẩn cấp.
Bên cạnh đó, Nanogen đã ký các thỏa thuận chuyển giao công nghệ sản xuất Nanocovax với hai đối tác Ấn Độ và Hàn Quốc vào ngày 10 và 20/8. Trong đó, đối tác Hàn Quốc sẽ sản xuất và phân phối vaccine ở quy mô toàn cầu, trừ Việt Nam và Ấn Độ. Ở trong nước, tỉnh Đồng Tháp đã giao một công ty đặt trước 200.000 liều vaccine Nanocovax.
VNE